Tóm tắt
Nghiên cứu tuyển chọn được chủng vi khuẩn Bacillus spp. S1, phân lập từ đường ruột tôm sú trưởng thành, có khả năng đối kháng với vi sinh vật kiểm định gồm Vibrio parahaemotilycus, Vibrio fluvialis và Vibrio cholerae. Sau 72 giờ nuôi cấy trên môi trường thạch ở điều kiện nhiệt độ 30C, đường kính vòng ức chế xuất hiện quanh điểm cấy Bacillus spp. đối với 3 vi sinh vật kiểm định trên lần lượt là 37,33cm±0,67; 35,00cm±2,88; 26,00cm±4,04. Thí nghiệm đánh giá khả năng kiểm soát Vibrio parahaemolyticus gây bệnh cho ấu trùng tôm Sú trong điều kiện in vivo cho thấy sự hiện diện của chủng vi khuẩn Bacillus spp. S1 trong môi trường nước nuôi ấu trùng tôm đã nhiễm V. parahaemotilycus khiến tỉ lệ sống sót của ấu trùng tôm Sú đạt 74% và tăng 14,67% so với đối chứng là 59,33%.
Từ khoá: Bacillus, Vibrio parahaemotilycus, Vibrio fluvialis, Vibrio cholerae, probiotics
1. Đặt vấn đề
Trong vài thập kỷ qua, nuôi trồng thuỷ sản đã trở thành ngành phát triển nhanh nhất thế giới trong lĩnh vực sản xuất lương thực thực phẩm, với tốc độ tăng trưởng hàng năm về nuôi tôm đạt 16,8%. Trong khi đó, theo báo cáo của Ngân hàng Thế giới, thiệt hại toàn cầu do bệnh tôm ước khoảng 3 tỷ USD. Những hậu quả tiêu cực của việc sử dụng kháng sinh trong nuôi trồng thuỷ sản là sự xuất hiện các chủng vi khuẩn kháng thuốc, giảm hiệu quả sử dụng kháng sinh kháng bệnh cho người và động vật. Từ thực tế này các phương pháp phòng bệnh thay thế được đề xuất như sử dụng các vi khuẩn như các tác nhân kiểm soát sinh học hoặc làm cân bằng hệ vi sinh vật trong môi trường ương nuôi ấu trùng tôm nhờ các vi sinh không gây bệnh có nguồn gốc từ môi trường tự nhiên [3,4].
Vi khuẩn thuộc chi Bacillus phân bố rộng rãi trong tự nhiên (đất, nước, không khí, thực phẩm), với khoảng gần 500 loài và dưới loài. Do sự đa dạng sinh thái và đa dạng loài như vậy các hoạt chất sinh học của chúng cũng vô cùng phong phú. Hơn nữa, Bacillus là thành phần chủ yếu trong hệ vi sinh vật ở mang, da và đường ruột của tôm [10]. Bacillus spp. thường thể hiện khả năng đối kháng với các vi sinh vật khác bao gồm các vi khuẩn gây bệnh ở tôm và động vật hai mảnh vỏ [8,9]. Sử dụng Bacillus như chế phẩm probiotics trong nuôi ấu trùng tôm đã thực hiện trong một số các nghiên cứu [7,12,13]. Khi sử dụng probiotics có bổ sung Bacillus S11, một chủng phân lập từ đường ruột của tôm Sú thu nhận ở Vịnh Thái Lan, kết hợp với ozon cho thấy tỉ lệ sống sót của tôm Sú tăng lên đáng kể so với đối chứng [5]. Bào tử của Bacillus đã được sử dụng như tác nhân kiểm soát sinh học để giảm vi khuẩn thuộc nhóm vibrios trong các ao nuôi tôm [8,11].
Nghiên cứu này đánh giá khả năng đối kháng của các chủng vi khuẩn Bacillus spp. đối với vi khuẩn Vibrio gây bệnh ở tôm Sú ở điều kiện in vitro và in vivo.
2. Nguyên liệu và Phương pháp nghiên cứu
2.1. Nguyên liệu nghiên cứu
56 chủng vi khuẩn Bacillus spp. trong Bộ sưu tập VSV phân lập từ rừng ngập mặn khu vực miền Trung của Bộ môn Công nghệ Sinh học - Vi sinh, Khoa Sinh học, Trường Đại học Sư phạm Hà Nội và 8 chủng vi khuẩn phân lập từ các mẫu ruột tôm Sú (Penaeus monodon) đã trưởng thành được sử dụng trong nghiên cứu này. Các chủng vi khuẩn kiểm định được sử dụng trong nghiên cứu này gồm Vibrio cholerae, Vibrio fluvialis, Vibrio parahaemolyticus do Bộ môn Công nghệ Sinh học - Vi sinh, Khoa Sinh học, Trường Đại học Sư phạm Hà Nội cung cấp.
Ấu trùng tôm Sú (Penaeus monodon) 1,5 tháng tuổi.
Các hoá chất được sử dụng trong nghiên cứu này đều ở mức độ phân tích.
2.2. Phương pháp nghiên cứu
Phương pháp xác định số lượng tế bào vi khuẩn trong môi trường dịch thể [1] Dùng pipette vô trùng lấy 1mL môi trường Nutrient Broth – NB (thành phần gồm cao thịt 3g/L; Pepton: 5g/L; NaCl: 8g/L với pH 7,5) nuôi cấy tế bào vi khuẩn nghiên cứu trong 24 giờ pha loãng theo phương pháp pha loãng giới hạn. Dùng pipette vô trùng hút lấy 100µl dịch ở độ pha loãng xác định trải đều trên môi trường Nutrient agar 1,5% thạch – NA (thành phần tương tự môi trường NB nhưng bổ sung 15g agar cho 1L môi trường) trong đĩa Petri. Các vi sinh vật nghiên cứu được giữ ở 30C trong 24 – 48 giờ. Xác định số lượng khuẩn lạc phát triển trong mỗi đĩa Petri thí nghiệm, từ đó xác định được số lượng tế bào vi khuẩn trong 1 mL dịch nuôi cấy ban đầu theo công thức: N = 1000.A/n.Df
Trong đó: N là tổng số tế bào trong 1mL dịch nuôi cấy ban đầu; A là số khuẩn lạc trung bình đếm được trên mỗi đĩa Petri; Df là độ pha loãng dịch huyền phù.; n là thể tích dịch pha loãng đem cấy trên mỗi đĩa Petri (100µl).
Đánh giá khả năng ức chế của các chủng vi khuẩn Bacillus spp. đối với Vibrio [6]
Phương pháp cấy đường chữ thập trên môi trường thạch đĩa: Khả năng đối kháng của vi khuẩn Bacillus spp., đối với các chủng Vibrio được kiểm tra trên môi trường NA1,5% thạch vô trùng bằng phương pháp cấy đường chữ thập. Sau đó, các hộp lồng thí nghiệm được ủ ở 30C trong thời gian 96 giờ.
Phương pháp xác định vòng vô khuẩn trên môi trường thạch đĩa: Các chủng Bacillus spp. được cấy chấm điểm trên 3 đĩa thạch chứa môi trường NA1,5% thạch giữ ở nhiệt độ 30C trong 24, 48 và 72 giờ. Chủng Vibrio tạo cặp đối kháng với Bacillus spp. theo phương pháp cấy chữ thập ở trên nuôi cấy trong 0,2 mL môi trường NB, ở 30C được bổ sung và trộn đều với 20 mL môi trường NA1,5% vô trùng và làm nguội đến nhiệt độ 40-45C. Hỗn hợp này được đổ nhẹ lên trên bề mặt hộp lồng chứa môi trường NA 1,5% thạch đã cấy chấm điểm Bacillus spp. trước đó. Sau 24-48 giờ ủ ở 30C, xác định và đo đường kính của các vòng vô khuẩn xuất hiện xung quanh điểm cấy Bacillus spp. được nuôi cấy trong 24, 48 và 72 giờ trên các hộp lồng.
Phương pháp xác định khả năng ức chế sự sinh trưởng của các vi khuẩn Vibrio trên môi trường dịch thể: Vi khuẩn Bacillus spp. S1 nghiên cứu được nuôi lắc trong môi trường NB với tốc độ 160 vòng/phút, ở 30C trong 72 giờ. Thu dịch nuôi cấy và ly tâm loại bỏ sinh khối ở 4000 vòng/phút trong 10 phút. Dùng pipette hút lấy 200µL dịch ly tâm đưa vào mỗi bình tam giác chứa 10mL môi trường NB đã bổ sung 200µL dịch nhân giống các chủng Vibrio và nuôi lắc với tốc độ 160 vòng/phút ở 30C trong 24 giờ. Số lượng tế bào Vibrio trong môi trường trước và sau khi bổ sung dịch ly tâm được xác định bằng phương pháp đếm khuẩn lạc như trên.
Đánh giá khả năng ức chế của chủng vi khuẩn Bacillus spp. tuyển chọn đối với chủng Vibrio gây bệnh trên ấu trùng tôm Sú trong điều kiện in vivo
Ấu trùng tôm Sú (Penaeus monodon) 1,5 tháng tuổi được chia vào 12 bể có thể tích 6L chứa 3L nước biển đã thanh trùng (50 ấu trùng/bể). Mỗi công thức thí nghiệm được lặp lại 3 lần nghĩa là gồm 3 bể thí nghiệm.
Công thức 1: không bổ sung vi sinh vật; Công thức 2: bổ sung 6 mL dịch nhân giống 1 ngày tuổi của V. parahaemolyticus; Công thức 3: bổ sung 6 mL dịch nhân giống 1 ngày tuổi của chủng Bacillus spp. đã tuyển chọn được; Công thức 4: bổ sung 6 ml dịch nhân giống 1 ngày tuổi của Bacillus spp. và 6 mL dịch nhân giống 1 ngày tuổi của chủng V. parahaemolyticus.
Các bể thí nghiệm đặt ở nhiệt độ phòng và ấu trùng tôm được cho ăn 2 lần/ngày (sáng và chiều) bằng thức ăn tổng hợp không chứa kháng sinh. Thông thường lượng thức ăn bằng 7% tổng khối lượng cơ thể ấu trùng tôm/bể. Lượng thức ăn có thể được điều chỉnh nếu thấy thức ăn thừa nhiều trong bể nuôi sau mỗi ngày. Các bể nuôi được sục khí liên tục nhằm cung cấp O2 bằng hệ thống sục khí mini. Sau khi bổ sung dịch nuôi cấy vi khuẩn, quan sát và đếm số tôm sống sót ở các bể thí nghiệm trong mỗi lô tại các thời điểm 3 ngày, 5 ngày và 7 ngày nuôi. Thời gian thí nghiệm kéo dài 7 ngày. Trước khi tiến hành thí nghiệm ấu trùng tôm được nuôi 7 ngày trong các bể với nước biển đã thanh trùng để làm quen với môi trường.
3. Kết quả Nghiên cứu và Thảo luận
3.1. Khả năng ức chế của các chủng Bacillus spp. nghiên cứu đối với Vibrio
Kết quả kiểm tra khả năng đối kháng Vibrio của các chủng Bacillus spp. bằng phương pháp cấy đường chữ thập cho thấy (hình 1):
Trong số 8 chủng vi khuẩn Bacillus spp. phân lập từ ruột tôm có 1 chủng (chiếm 12,5%) thể hiện khả năng đối kháng với cả 3 chủng V. cholerae, V. fluvialis, V. parahaemotilycus gây bệnh trên tôm.
Trong số 56 chủng vi khuẩn Bacillus spp. của Bộ môn Công nghệ Sinh học - Vi sinh chúng tôi thấy có 8 chủng vi khuẩn (chiếm 14,3%) có khả năng đối kháng với các chủng Vibrio gây bệnh.
Nghiên cứu trên tôm sú ở vịnh Thái Lan cho thấy Bacillus và Vibrio là hai nhóm vi khuẩn chiếm ưu thế khi phân lập từ đường ruột của tôm sú bố mẹ [8]. Một nghiên cứu trên ruột tôm sú nuôi thâm canh tại Cà Mau, Việt Nam cũng cho kết quả tương tự [2].
Bảng 1. Khả năng đối kháng của các chủng Bacillus spp.
với V. parahaemotilycus, V. fluvialis và V. cholerae
|
Kí hiệu chủng
vi khuẩn
|
Đường kính vòng vô khuẩn(TB ± SD)(mm)
|
||
|---|---|---|---|
|
24 giờ
|
48 giờ
|
72 giờ
|
|
|
V. parahaemotilycus
|
|||
|
S1
|
26,0 ± 0,58
|
28,66 ± 1,76
|
37,33 ± 0,67
|
|
MT1
|
18,33 ± 1,45
|
26,33 ± 1,76
|
20,33 ± 1,45
|
|
MT48
|
20,67 ± 0,33
|
24,67 ± 0,58
|
24,00 ± 0,58
|
|
MT52
|
17,33 ± 0,88
|
27,33 ± 0,58
|
20,67 ± 0,33
|
|
MT72
|
18,67 ± 0,33
|
23,67 ± 1,76
|
21,00 ± 0,58
|
|
MT80
|
20,33 ± 0,33
|
31,33 ± 1,33
|
31,33 ± 1,76
|
|
MT81
|
21,33 ± 1,76
|
24,33 ± 1,86
|
28,33 ± 1,86
|
|
MT84
|
24,33 ± 1,45
|
26,67 ± 2,33
|
25,67 ± 2,33
|
|
V. fluvialis
|
|||
|
S1
|
23,67 ± 0,33
|
33,67 ± 0,33
|
35,00 ± 2,88
|
|
MT48
|
15,00 ± 1,52
|
21,00 ± 1,52
|
24,33 ± 0,67
|
|
MT52
|
11,33 ± 1,76
|
15,00 ± 0,58
|
22,33 ± 1,20
|
|
MT70
|
18,33 ± 1,20
|
25,33 ± 1,76
|
30,33 ± 1,33
|
|
MT72
|
17,00 ± 0,58
|
20,33 ± 0,33
|
22,33 ± 1,45
|
|
MT80
|
19,67 ± 2,33
|
20,00 ± 0,58
|
12,00 ± 0,58
|
|
MT84
|
17,33 ± 2,03
|
25,33 ± 2,67
|
29,00 ± 1,53
|
|
V. cholerae
|
|||
|
S1
|
23,33 ± 0,88
|
23,67 ± 2,67
|
26,00 ± 4,04
|
|
MT48
|
16,67 ± 1,20
|
21,67 ± 0,67
|
24,00 ± 3,21
|
Thí nghiệm kiểm tra khả năng ức chế của các chủng Bacillus spp đối với vi khuẩn Vibrio trên môi trường thạch (bảng 1 và hình 2) cũng cho kết quả tương tự khi sử dụng phương pháp cấy chữ thập (hình 1). Trong số các chủng Bacillus spp. nghiên cứu, chủng vi khuẩn mang kí hiệu S1 thể hiện hoạt tính đối kháng mạnh mẽ đối với cả 3 chủng Vibrio. Đây là chủng phân lập được từ đường tiêu hoá của tôm Sú nên mang lợi thế về khả năng thích nghi trong môi trường ruột tôm khi được tuyển chọn làm probiotics. Việc sử dụng các vi sinh vật không gây bệnh có nguồn gốc từ môi trường tự nhiên như các yếu tố kiểm soát sinh học trong ương nuôi thuỷ sản là một trong những phương pháp phòng bệnh nhiều triển vọng [3,4]. Với những đặc tính như vậy, chủng vi khuẩn Bacillus spp. S1 được lựa chọn cho các nghiên cứu tiếp theo.
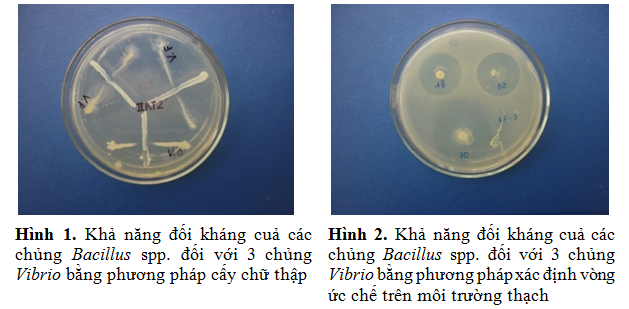
Hoạt tính đối kháng của các chủng Bacillus spp. đối với các chủng Vibrio thể hiện mạnh hơn sau 48 giờ và 72 giờ thí nghiệm. Vì hoạt chất ức chế sinh trưởng đối với các chủng Vibrio sinh bởi Bacillus spp. có thể trong các pha sinh trưởng sau của chu kì sinh trưởng vi khuẩn.
Tất cả các thí nghiệm trên của chúng tôi đều thực hiện trên môi trường thạch đĩa. Để ứng dụng có hiệu lực cao trong môi trường nước nuôi tôm chúng tôi kiểm tra khả năng đối kháng của vi khuẩn Bacillus spp. với Vibrio trên môi trường dịch thể.
Do thời gian có hạn chúng tôi mới chỉ kiểm tra được khả năng đối kháng của chủng Bacillus spp. S1, chủng thể hiện hoạt tính đối kháng tốt nhất đối với 3 vi sinh vật kiểm định, với một loại Vibrio gây bệnh (V. parahaemolyticus) trong môi trường dịch thể. Số lượng tế bào V. parahaemotilycus phát triển trong môi trường dịch thể trước và sau khi bổ sung dịch nuôi cấy chủng Bacillus spp. S1 được thể hiện trong bảng 2.
Bảng 2. Khả năng ức chế V. parahaemotilycus của chủng Bacillus spp. S1
trên môi trường dịch thể
|
Thời gian thí nghiệm
|
Số lượng TB/mL của chủng V. parahaemotilycus
(´105)
|
|
0 giờ
|
2,3
|
|
24 giờ
|
1,04
|
Từ kết quả thấy sau 24 giờ tỉ lệ chủng V. parahaemotilycus bị ức chế bởi dịch nuôi cấy của Bacillus spp. S1 là 54,78%.
3.2. Khả năng ức chế của chủng vi khuẩn Bacillus spp. tuyển chọn đối với chủng Vibrio gây bệnh trên ấu trùng tôm Sú trong điều kiện in vivo
Vibrio gây bệnh trên tôm đã trở thành vấn nạn của nghề nuôi tôm ở nước ta. Nhiều cơ sở nuôi tôm đã bị thiệt hại nghiêm trọng bởi dịch bệnh do Vibrio, virut đốm trắng và bệnh MBV (Monodon Bacuro Virus) gây ra hiện tượng tôm chết hàng loạt. Do có hạn về mặt thời gian nên chúng tôi chưa kiểm tra được khả năng kiểm soát của chủng Bacillus spp. S1 đối với mỗi loại Vibrio gây bệnh. Trong số 3 chủng Vibrio chúng tôi dùng trong nghiên cứu này, chúng tôi chỉ tiến hành nghiên cứu khả năng ức chế của chủng S1 đối với chủng V. parahaemolyticus trên ấu trùng tôm Sú (Penaeus monodon) 1,5 tháng tuổi ở quy mô phòng thí nghiệm.
Kết quả thử nghiệm khả năng ức chế V. parahaemolyticus của chủng S1 trên ấu trùng tôm Sú (Penaeus monodon) ở quy mô phòng thí nghiệm được trình bày trong bảng 3.
Bảng 3. Khả năng ức chế V. parahaemolyticusgây bệnh
trên ấu trùng tôm Sú (Penaeus monodon)1,5 tháng tuổi của chủng Bacillus spp. S1
|
Công thức
|
Tỉ lệ sống sót của tôm (%)
|
||
|---|---|---|---|
|
3 ngày
|
5 ngày
|
7 ngày
|
|
|
Công thức 1
|
100
|
91,33
|
86,67
|
|
Công thức 2
|
100
|
66
|
59,33
|
|
Công thức 3
|
100
|
91,33
|
86
|
|
Công thức 4
|
100
|
80
|
74
|
Công thức 1 (đối chứng): trong điều kiện không bổ sung vi sính vật gây bệnh cũng như Bacillus spp. khả năng sống sót của ấu trùng tôm Sú tại thời điểm ngày thứ 5 đạt 91,33%, sang đến ngày thứ 7 tỉ lệ này còn 86,67%. Số lượng ấu trùng tôm giảm dần theo thời gian nuôi trong công thức 1 do trong quá trình sinh trưởng của tôm các sản phẩm chuyển hóa được sinh ra có thể có ảnh hưởng tiêu cực đến chất lượng nước trong các bể. Trong suốt 7 ngày tiến hành thí nghiệm nước trong các bể không được thay. Ở công thức 2 với sự hiện diện của V. parahaemolyticus, sau 5 ngày tỷlệ sống sót đạt 66% và đến ngày thứ 7 số lượng ấu trùng tôm chết tiếp tục tăng lên đồng nghĩa tỷ lệ sống sót giảm chỉ còn 59,33%. Như vậy khi so với các công thức thí nghiệm khác, đây là công thức có tỷ lệ sống sót của ấu trùng tôm Sú thấp nhất. Vi khuẩn V. parahaemolyticusxuất hiện trong bể nuôi đã có những tác động tiêu cực đến sức sống của ấu trùng tôm. Kết quả tỷ lệ ấu trùng tôm chết trong công thức thí nghiệm 3 ở thời điểm ngày thứ 5 là tương đươngvới công thức 1 (91,33%). Tương tự tại thời điểm 7 ngày, tỷlệ sống sót của ấu trùng tômđạt 86% không khác biệt đáng kể với giá trị này 86,67% của công thức 1, nhưng vẫn cao hơn so với hai công thức 2, 4. Như vậy việc bổ sung vi khuẩn Bacillus spp. S1 vào môi trường nuôi ấu trùng tôm chưa gây ra những ảnh hưởng tiêu cực đến sức sống của ấu trùng tôm thí nghiệm.Ở công thức 4 dịch nuôi cấy Bacillus spp. S1 và dịch nuôi cấy V. parahaemolyticus được bổ sung vào các bể nghiên cứu. Tại thời điểm ngày thứ 5, tỷ lệ sống sót của ấu trùng tôm đạt 80% cao hơn 14% so với công thức 2. Tỷ lệ sống sót của tôm tại thời điểm 7 ngày là 74% cao hơn so 14,67% khi so với công thức 2 (59,33%), nhưng thấp hơn 12,67% so với công thức 1 (86,67%). Kết quả này cho thấy việc sử dụng đơn chủng vi khuẩn Bacillus spp. S1 đã kiểm soát một phần vi khuẩn V. parahaemolyticusgây bệnh trên ấu trùng tôm Sú. Tuy nhiên, để đạt hiệu quả kiểm soát vi sinh vật gây bệnh của chế phẩm probitics, việc nghiên cứu phối hợp chủng Bacillus spp. S1 với những chủng vi sinh vật khác là cần thiết trong nghiên cứu tiếp theo. Mặt khác, mật độ vi khuẩn Bacillus spp. bổ sung vào thí nghiệm có thể chưa đủ để ức chế hoàn toàn V. parahaemolyticus.
Kết luận
Nghiên cứu đã tuyển chọn được chủng Bacillus spp. S1, phân lập từ đường ruột tôm sú trưởng thành, có khả năng đối kháng với 3 vi sinh vật kiểm định V. parahaemotilycus, V. fluvialis vàV. cholerae. Sau 72 giờ nuôi cấy trên môi trường NA 1,5% thạch, đường kính vòng ức chế đối với 3 vi sinh vật kiểm định trên lần lượt là 37,33cm±0,67; 35,00cm±2,88; 26,00cm ± 4,04.Thí nghiệm đánh giá khả năng kiểm soát V. parahaemolyticus gây bệnh cho ấu trùng tôm Sú trong điều kiện in vivo cho thấy sự hiện diện của chủng vi khuẩn Bacillus spp. S1 trong môi trường nước nuôi ấu trùng tôm đã nhiễm V. parahaemotilycuskhiến tỉ lệ sống sót của ấu trùng tôm Sú đạt 74% và tăng 14,67% so với đối chứng là 59,33%. Tuy nhiên để tăng cường hiệu quả của probiotics, cần nghiên cứu phối hợp chủng S1 với một số chủng vi sinh vật có tiềm năng probiotics.
Tài liệu tham khảo
[1] Trần Linh Thước, 2006. Phương pháp phân tích vi sinh vật trong nước, thực phẩm và mĩ phẩm. NXB Giáo dục; 50-67
[2] Phạn Thị Tuyết Ngân và Nguyễn Hữu Hiệp, 2010. Biến động mật độ vi khuẩn hữu ích trong ao nuôi tôm Sud (Penaeus monodon) thâm canh. Tạp chí Khoa học Trường Đại học Cần Thơ; 14: 166-176.
[3] Defoirdt T, Boon N, Sorgeloos P, Verstraete W, Bossier P, 2007. Alternatives to antibiotics to control bacterial infections: luminescent vibriosis in aquaculture as an example. Trends in Biotechnology; 25: 472-479.
[4] Guo JJ, Liu KF, Cheng SH, Chang CI, Lay JJ and Hsu YO, 2009. Selection of probiotic bacteria for use in shrimp larviculture. Aquaculture Research; 40: 609-618.
[5] Meunpol, O., K. Lopinyosiri, and P. Menasveta. 2003. The effects of ozone and probiotics on the survival of black tiger shrimp (Penaeus monodon). Aquaculture; 220: 437–448.
[6] Purivirojkul W and Areechon N, 2007. Application of Bacillus spp. isolated from the intestine of black tiger shrimp (Penaeus monodon Fabricius) from natural habitat for control pathogenic bacteria in aquaculture. Kasetsart University Research and Development Institute; 125-132.
[7] Ramesh K, Natarajan M, Sridhar H, Uma Vanitha M and Umamaheswari S, 2014. Feasibility of shrimp gut probionts with anti-vibrio and anti-qs in penaeid culture. International Journal of Fisheries and Aquatic Studies; 1(3): 26-34
[8] Rengipipat S, Rukpratanporn S, Piyatiratitivorakul S and Menasaveta P, 2000. Immunity enhancement in black tiger shrimp (Penaeus monodon) by a probiont bacterium (Bacillus S11). Aquaculture; 191: 271–288.
[9] Rengpipat S, Tunyanun A, Fast A, Piyatiratitivorakul S and Menasveta P, 2003. Enhanced growth and resistance to Vibrio challenge in pond-reared black tiger shrimp Penaeus monodon fed a Bacillus probiotic. Diseases of Aquatic Organisms; 55: 169-173.
[10] Sharmila R, Jawahar Abraham T and Sundararaj V, 1996. Bacterial flora of semi-intensive pond reared Penaeus indicus (H.Milne Edwards) and the environment. Journal of Aquaculture in the Tropics; 11: 193–203.
[11] Skjermo J, and Vadstein O, 1999. Techniques for microbial control in the intensive rearing of marine larvae. Aquaculture; 177: 333–343.
[12] Vaseeharan B and Ramasamy P, 2003. Control of pathogenic Vibrio spp. by Bacillus subtilis BT23, a possible probiotic treatment for black tiger shrimp Penaeus monodon. Letters in Applied Microbiology; 36: 83–87.
[13] Vine NG, Leukes WD and Kaiser H, 2006. Probiotics in marine larviculture. FEMS Microbiology Reviews; 30: 404-427.
Screening Bacillus spp. having inhibitory ability against pathogenic Vibrio in black tiger shrimp larvae (Penaeus monodon) to produce potential probiotics
Phan Due Thanh, Nguyen Thi Hien và Tong Thi Mo
Department of Biotechnology and Microbiology, Faculty of Biology, HNUE
Abstract
In this study, selected Bacillus spp. S1, isolated from gut tracts of healthy adult tiger shrimps, performed potentially antagonistic affects against the growth of pathogenic bacteria Vibrio including Vibrio parahaemotilycus, Vibrio fluvialis and Vibrio cholerae. After 72 hours of culturing on NA 1.5% agar at temperatures of 30°C, diameters of inhibitory zone against the growth of the 3 mentioned Vibrio species were 37.33cm±0.67; 35.00cm±2.88; 26.00cm±4.04, respectively. The co-cultured experiment evaluated the ability to control pathogenic Vibrio under in vivo revealed that the presence of Bacillus spp. S1 made the survival rate of the tiger prawn larvae, which were exposed to V. parahaemotilycus, reached 74% and increased 14,67% compared with 59.33% of the control.
Keywords: Bacillus, Vibrio parahaemotilycus, Vibrio fluvialis, Vibrio cholerae, probiotics

